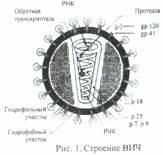
ВИЧ/СПИД этиология, патогенез, клинические симптомы, диагностика, лечение
СПИД
Синдром приобретенного иммунодефицита (СПИД) — важнейшая мировая медицинская, социальная и политическая проблема ХХ века. Середину 1981 г. можно считать началом эпидемии СПИД. Вирус иммунодефицита человека — ВИЧ относится к подсемейству лентивирусов, семейства ретровирусов, РНК-содержащих, и имеющих ферменты — обратную транскриптазу (ревертазу), интегразу, протеазу. При попадании ВИЧ в живую клетку РНК под воздействием ревертазы превращается в ДНК, которая встраивается в ДНК клетки-хозяина, продуцируя новые вирусные частицы-копии РНК вируса, оставаясь в клетке пожизненно. Ядро клетки окружено оболочкой, содержащей гликопротеид gp120, обуславливающий прикрепление вируса к клеткам организма человека, имеющим рецептор CD4. Этот рецептор несут в основном клетки, циркулирующие в крови, лимфе и тканевой жидкости, а также относящиеся к неспецифическим элементам нервной ткани. Новые вирусные частицы атакуют клетки, вызывая их гибель, нарушая их взаимодействие с другими клетками, что ведет к прогрессирующим нарушениям иммунитета. Большое количество циркулирующих в крови вирусных частиц определяет вероятность быстрого снижения количества иммунных клеток. Учитывая четкую связь между развитием заболевания и снижением у больного количества CD4-лимфоцитов, ученые полагают, что их снижение является главной особенностью патогенеза СПИД. Нарушается также функция лимфоцитов хелперов/индукторов, что приводит к спонтанной активации В-клеток и развитию поликлональной гипергаммаглобулинемии за счет продукции неспецифических иммуноглобулинов. Как следствие, повышается концентрация циркулирующих иммунных комплексов. В результате сдвигов иммунитета снижается сопротивляемость к вторичным инфекциям и опухолям. За счет прямого цитопатического действия вируса или в результате опосредованного действия (аутоиммунные механизмы) возможно поражение клеток нервной системы и различных клеток системы крови, сердечно-сосудистой, костно-мышечной, эндокринной и других систем. На процессы, обусловленные действием ВИЧ, накладывается широкий спектр процессов, вызываемых развившимися вторичными заболеваниями. Все это обуславливает полиорганность поражений и разнообразие клинической симптоматики.
В настоящее время известны два типа вируса — ВИЧ-1 и ВИЧ-2, различающиеся по своим структурным и антигенным характеристикам. Имеются достоверные различия в течении заболевания, вызываемого этими вирусами. Течение инфекции, вызываемой ВИЧ-2, считается более продолжительным. Среди ВИЧ-1 и ВИЧ-2 выделяют большое число генетически различных групп. Как и все ретровирусы, вирус ВИЧ характеризуется высокой изменчивостью. Считается, что в организме человека по мере прогрессирования инфекции, от бессимптомной до манифестной, происходит эволюция вируса от менее вирулентного к более вирулентному варианту. ВИЧ нестоек во внешней среде, чувствителен к внешним воздействиям, практически полностью инактивируется при нагревании выше 56°С в течение 30 мин, погибает при кипячении через 1-3 мин, а также под воздействием дезинфицирующих средств (3%-ный раствор перекиси водорода, 5%-ный раствор лизола, 70%-ный — этилового спирта). Возможно его сохранение во внешней среде в жидкостях, содержащих вирус в высоких концентрациях, таких как кровь и сперма. Губительны для ВИЧ солнечное и искусственное УФ-излучение, а также все виды ионизирующего излучения. В крови, предназначенной для переливания, вирус живет годы, в замороженной сперме несколько месяцев. Появились данные о том, что ВИЧ теряет активность под воздействием защитных ферментов, содержащихся в слюне и поте. Передачи ВИЧ при укусах кровососущих насекомых не происходит.
Пути передачи ВИЧ-инфекции: половой, парентеральный, вертикальный. Половой путь передачи реализуется при гетеросексуальных и гомосексуальных половых контактах. Вероятность заражения повышается при воспалительных заболеваниях половых органов. Парентеральный путь инфицирования встречается в основном среди инъекционных наркоманов. Факторами передачи ВИЧ при этом могут быть общие шприцы и иглы, наркотик, в который добавляется кровь. Инфицирование возможно при переливании зараженной крови, ее препаратов, использовании загрязненных кровью медицинских инструментов, не прошедших соответствующую обработку. Факторами передачи вируса могут быть органы и ткани доноров, используемых для трансплантации. Если женщина заражена ВИЧ, то вероятность инфицирования плода составляет около 50%. Ребенок может инфицироваться до, во время и после родов. Контактно-бытовой и воздушно-капельный пути передачи при ВИЧ-инфекции не встречаются.
ВИЧ-инфекция характеризуется многолетним течением, клинически связанным с прогрессирующим снижением иммунитета и приводящим к развитию тяжелых форм оппортунистических заболеваний. До настоящего времени считалось, что в большинстве случаев ВИЧ-инфекция имеет единственный исход — гибель зараженного ВИЧ организма. Однако теория инфекционного процесса допускает существование как маловирулентных или дефектных штаммов ВИЧ, так и устойчивых к инфекции больных. Среднюю продолжительность жизни инфицированного человека оценивают сейчас в 12 лет, однако продолжительность болезни может быть связана с путями заражения, принадлежностью к различным группам населения, возрастом, расовыми особенностями и доступностью медицинской помощи.
Течение ВИЧ-инфекции многие исследователи пытались отобразить с помощью клинических классификаций. В нашей стране принята следующая классификация ВИЧ-инфекции (В. И. Покровский, 1989).
I. Стадия инкубации.
II. Стадия первичных проявлений:
А — острая лихорадочная фаза,
Б — бессимптомная фаза,
В — персистирующая генерализованная лимфоаденопатия.
III. Стадия вторичных заболеваний:
А — потеря массы тела менее 10%, поверхностные грибковые, бактериальные, вирусные поражения кожи и слизистых оболочек, опоясывающий лишай, повторные фарингиты, синуситы,
Б — прогрессирующая потеря массы тела более 10%, необъяснимая диарея или лихорадка более 1 месяца, волосатая лейкоплакия, туберкулез легких, повторные или стойкие бактериальные, грибковые, вирусные, протозойные поражения внутренних органов (без диссеминации) или глубокие поражения кожи и слизистых оболочек, повторный или диссеминированный опоясывающий лишай, локализованная саркома Капоши,
В — генерализованные бактериальные, вирусные, грибковые, протозойные и паразитарные заболевания, пневмоцистная пневмония, кандидоз пищевода, атипичный микобактериоз, внелегочный туберкулез, кахексия, диссеминированная саркома Капоши, поражения ЦНС различной этиологии.
IV. Терминальная стадия.
Выделяют также три иммунологические категории в зависимости от уровня СД4-лимфоцитов:
1) более 0,5 х 109/л СД4-клеток в 1 мм3 крови,
2) от 0,2 до 0,5 х 109/л в 1 мм3,
3) менее 0,2 х 109/л в 1 мм3.
Таким образом, каждый больной может быть отнесен к той или иной категории по клиническим и иммунологическим критериям. В данной классификации учитываются все проявления болезни от момента заражения до гибели больного, включая и те, которые, возможно, еще неизвестны.
Клиническая картина.
Инкубационный период при ВИЧ – инфекции длится от нескольких месяцев до 3-5 лет и даже больше. Чаще всего в продромальном периоде имеет место лихорадка неясного генеза, похудание, диарея, утомляемость, ночные поты и развивается персистирующая или постоянная лимфаденопатия. Стабильное увеличение лимфоузлов является первым признаком расстройства иммунной системы. Обычно увеличены шейные, подмышечные, подчелюстные и другие лимфоузлы, причём диагностическое значение имеет увеличение не менее двух групп их вне паховой области. Лимфатические узлы умеренно болезненны (или безболезненны), не связаны с клетчаткой, подвижны, размером от 0,5 до 3 см в диаметре.
В этой стадии ВИЧ – инфекции дифференциальная диагностика сложна, так как увеличение лимфатических узлов наблюдается при многих инфекционных и неинфекционных заболеваниях: инфекционном мононуклеозе, краснухе, лимфогранулематозе, лейкозе, туберкулёзе. Увеличение подчелюстных и переднешейных лимфоузлов может быть обусловлено заболеваниями зубов, верхних дыхательных путей. Дифференциальная диагностика проводится путём исключения этих заболеваний.
Эксперты ВОЗ считают, что увеличение нескольких групп лимфоузлов, длящееся более 1,5 мес., позволяет предполагать СПИД.
В дальнейшем клинические проявления при развёрнутом заболевании СПИДом очень многообразны и зависят, прежде всего, от того, каким микроорганизмом вызваны наслоившиеся инфекции у данного больного.
В соответствии с преимущественной локализацией очагов поражения и особенностями патогенеза заболевания выделяют несколько клинических форм СПИДа:
1) лёгочная – в 30-35% случаев протекает в сочетании с саркомой Капоши, характеризуется развитием интерстициальной пневмонии,
2) кишечная – обусловлена диарейным синдромом, характеризуется длительным течением (1-2 мес. И боле), существенной (10% и боле) потерей массы тела, частыми рецидивами, резистентностью к лечению бактериальными препаратами отсутствием в фекалиях «обычных» возбудителей диарейных заболеваний. Желудочно-кишечные нарушения проявляются вялотекущей диареей и часто осложняются геморрагиями, кишечной непроходимостью, перфорацией,
3) церебральная – наблюдается в виде изолированных опухолей мозга сравнительно не часто (лимфомы 2-3%). Чаще (у 15-20%больных) регистрируются различные втоичные инфекции ЦНС (менингиты, абсцессы мозга острые и подострые энцефалиты). Кроме того, в ряде случаев как следствие тромбоцитопении развиваются различные сосудистые поражения, церебральные геморрагии,
4) диссеминированная – встречается довольно часто (50-60%), проявляется поражением кожи слизистых оболочек,
5) недифференцированные формы – отличаются длительной (2-3 мес.) лихорадкой неясной этиологии, «беспричинной» потерей массы тела на 10% и более, длительной диареей (3-5 месяцев) без высева «обычных» возбудителей и при отсутствии эффекта от лечения, а также другими системными изменениями без определённой локализации патологического процесса. Эта группа больных требует обследования на ВИЧ – инфекцию.
Комитет экспертов ВОЗ разработал критерии для клинической диагностики СПИДа. О наличии больного этой инфекции свидетельствуют с большой вероятностью следующие признаки: 1) саркома Капоши лиц моложе 60 лет, 2) хронический диарейный синдром (более 1-2 месяцев) при отсутствии в фекалиях «обычных» энтеропатогенных микроорганизмов или наличии большого количества криптоспородий, 3) длительная лихорадка неясной этиологии, 4) лимфома ЦНС, 4) хронические пневмонии неясной этиологии, резистентные к обычной химиотерапии, пневмоцистная пневмония, 6) «беспричинное» снижение массы тела больного на 10% и более (если отсутствуют влияние алиментарного фактора или какие-либо тяжёлые соматические заболевания), 7) лимфопения нерасшифрованной этиологии, 8) эндогенные или экзогенные реинфекции или суперинфекции.
В то же время ряд признаков позволяет с достаточной определённостью исключить диагноз ВИЧ-инфекции: 1) генез выявленной иммунной недостаточность ясен, т.е. она детерминирована известными врачу факторами (предшествующей лучевой терапией, применением кортикостероидных гормонов, лечением иммунодепрессантами после пересадки органов или по поводу каких-либо заболеваний и т.д.), 2) иммунодефицит имеет первичную природу (генетически детерминированный, врождённый), 3) иммунная недостаточность развилась на соответствующем патогенетическом фоне, обусловленном тяжёлыми заболеваниями (например, злокачественными новообразованиями), выраженной белковой недостаточностью, метаболическими расстройствами и другими предшествующими патологическими изменениями.
При ВИЧ-инфицировании большое значение придаётся сопутствующим оппортунистическим инфекциям и онкогенным заболеваниям.
СПИД характеризуется присоединением малоинвазионных возбдителей и сапрофитов, получивших название оппортунистических, т.е. микробов-приспособленцев.
По этиологическому признаку все они делятся на следующие группы:
- Протозойные инфекции: 1) пневмоцисты, 2) криптоспородии, 3) токсоплазмозы,
- Грибковые заболевания: 1) аспергиллёз, 2) кандидоз, 3) криптококкоз,
- Бактериальные инфекции: атипичные микобактерии, реже патогенные, такие как сальмонеллы (которые имеют склонность к генерализации и рецидивам), стафилококк и др.,
- Вирусные заболевания: 1) цитомегаловирусы, 2) простой герпес, 3) опоясывающий герпес, 4) вирусы Эпштейна-Барра, 5) легионеллы, 6) паповавирсы,
От первичных иммунодефицитов следует отличать вторичные. Последние вызываются различными факторами: травматическими, метаболическими нарушениями (в том числе диабетом, другими эндокринными заболеваниями), ятрогенными (цитостатики, антибиотики, гормоны), рентген- и радиационными облучениями.
При ВИЧ-инфекции нет классически очертанной клинической картины, следовательно она может протекать под «маской» ассоциированных с ней заболеваний, индуцированных иммунодефицитом. При ВИЧ_инфекции повреждаются различные органы и системы организма. Широкое «представительство» органной патологии и оппортунистических инфекций приводит к тому, что впервые встретиться с больным СПИДом может врач любого профиля.
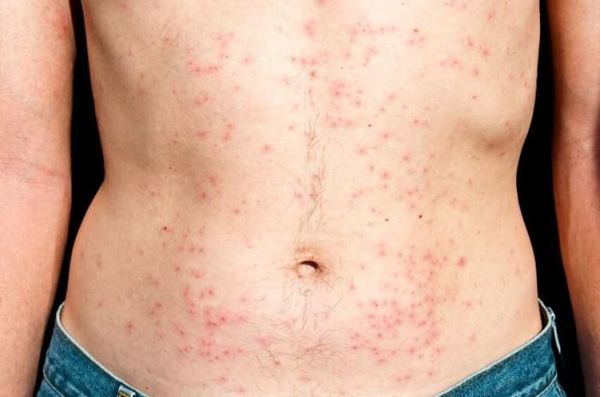
Ранними клиническими признаками стадии СПИДа является усиление симптомов предшествующего периода – продрома (преСПИДа): прогрессирует общая слабость, снижается масса тела, продолжается лихорадка, отсутствует аппетит, наблюдается лейкопения. Некоторых развивается заболевание, напоминающие инфекционный мононуклеоз. На ряду с общей слабостью и температурой увеличиваются миндалины, на теле иногда появляется пятнистая сыпь. Кроме того, зафиксированы органические симптомы со стороны ЦНС, которые включают диапазон от головных болей до энцефалита. В отличие от обычного инфекционного мононуклеоза лимфаденопатия при ВИЧ-инфекции принимает хроническое течение, в периферической крови отмечаются лимфопения и уменьшается количество Т4- лимфоцитов, в крови определяются антитела к ВИЧ.
Большинство оппортунистических инфекций возникает, когда у больных ВИЧ-инфекцией количество Т4- лимфоцитов резко снижается.
На первый план часто выступают заболевания дыхательного тракта. Особое место среди них принадлежит пневмоцистной пневмонии. Она выявляется в 64% наблюдений.
Вирус Эпштейна-Барра часто выявляется из глоточных смывов у больных ВИЧ-инфекцией, осложнённой лимфоидными опухолями или мононуклеозно увеличенными лимфоузлами.
Желудочно-кишечные расстройства (энтерит с потерей массы тела) характерны для кишечного криптоспоридоза. У больных обильный, профузный водянистый стул без примеси слизи и крови. Тенезмов и ложных позывов также не отмечается.
Причиной диарей больных ВИЧ-инфекцией, помимо словно-патогенной флоры, могут быть сальмонеллы, шигеллы и другие патогенные бактерии.
Психоневрологические изменения на ранней стадии ВИЧ-инфекции включает лёгкие нарушения познавательной функции, снижение критической оценки и памяти. Эти расстройства обусловлены как оппортунистическими инфекциями, так в равной мере могут быть результатом репликации ВИЧ в мозговых клетках с выделением церебротоксинов. На поздних стадиях болезни выявляются деменция, синдром, характеризующийся потерей точности мышления, затем присоединяется нарушение движения. Больные перестают общаться, утрачивают возможность ходить.
Для паповавирусной инфекции типична прогрессирующая многофокусная лейкоэнцефалопатия. Течение носит подострый характер. Клинические признаки выражены слабо: общее недомогание, сонливость, заторможенность, потеря интереса к работе, депрессия и слабоумие.
Поражения кожи и слизистых оболочек, учитывая их частоту и своеобразие клинической картины, могут быть наиболее ранним и чувствительным признаком ВИЧ-инфицирования. Одновременно они могут проявляться в стадии СПИДа, обусловленные оппортунистическими заболеваниями.
Самая частая форма поражения кожи при СПИДе – молниеносная, злокачественная или эпидемическая форма саркомы Капоши. Саркома Капоши отнесена к группе злокачественных опухолей кровеносных сосудов (ангиоретикулоэндотелиоз). Этиология заболевания неизвестна, но накапливаются свидетельства в пользу вирусной природы (мегаловирусы вирус Эпштейна-Барра, вирус простого герпеса), генетических факторов. Несомненна связь саркомы Капоши с иммунодефицитом любого происхождения.
Обращают на себя внимание высокая частота и атипичность течения вирусных поражений кожи у больных СПИДом. Простой пузырьковый лишай (простой герпес) появляется у них в 40-50 раз чаще, чем в соответствующей по возрасту популяции здоровых, и обнаруживается у 22-87%. Поражаются губы, слизистая полости рта, гениталии и перианальная область. Высыпания множественные, периодически рецидивируют, изъязвляются, склонны к затяжному течению, нередко осложняются кандидозом. Опоясывающий герпес обычно появляется в виде групп пузырьков по ходу нерва односторонне, при СПИДе нередки генерализованные формы. Высыпания сравнительно быстро подвергаются некрозу, изъязвляются, сопровождаются мучительными и стойкими невритами, могут рецидивировать.
Часто у больных мужчин обнаруживаются остроконечные кандиломы, которые обычно возникают в области венечной бороздки, на внутреннем листке крайней плоти и в перианальной области. При СПИДе они множественные, увеличенные в размерах, могут изъязвляться, упорны по отношению к терапии, принимают рецидивирующее течение.
У 11-25% больных СПИДом на боковых поверхностях языка появляются «волосатые» лейкоплакии – белесоватые бляшки с ворсинчатой поверхностью. Возникновение их некоторые авторы связывают с инвазией папилломатозного вируса, вируса герпеса и Эпштейна-Барра.
Дрожжеподобные микроорганизмы типа кандид – постоянные обитатели кожных покровов, слизистой полости рта и кишечника. При угнетении конкурентной флоры или снижении сопротивляемости организма они начинают усилено размножаться и вызывают развитие клинических проявлений кандидоза: ограниченных и распространённых и даже системных и, наконец, кандидозного сепсиса.
Лабораторная диагностика
Обследованию на ВИЧ-инфекцию в первую очередь подлежат:
1) Лица, у которых отмечается лихорадка неясного генеза, длительностью свыше 1 мес., увеличение лимфатических узлов двух и более групп продолжительностью свыше 1 мес., диарея длительностью свыше 1 мес., немотивированная потеря массы тела свыше 10%, повторные пневмонии в течение одного года, рецидивирующие гнойно-бактериальные или паразитарные заболевания, чсепсис, рецидивирующая пиодермия, волосатая" лейкоплакия языка,
2)Лица с клиникой кандидозного эзофагита, кандидоза бронхов и легких, диссеминированного или внелегочного кокцидиомикоза, пневмоцистной пневмонии, внелегочного криптококкоза, криптоспоридиоза с диареей юлительностью свыше 1 мес., цитомегаловирусного поражения внутренних органов кроме печени, селезенки, лимфатических узлов у больных старше 6 мес., цитмегаловируснго ретинита с потерей зрения, герпетической инфекции с многоочаговыми язвами длительностью свыше 1 мес., бронхитом, пневмонией или эзофагитом, рецидивирующего опоясывающего герпеса, дессиминированного или внелегочного гистоплазмоза, туберкулеза легких или внелегочного, изоспориоза с диареей длительностью свыше 1 мес., распространенной или внелегочной МАК-инфекции, прогрессирующей многофокусной лейкоэнцефалопатии, токсоплазмоза мозга, сальмонеллезной септицемии, саркомы Капоши, лимфомы, лимфоидной интерстициальной пневмонии (у детей).
Лабораторная диагностика ВИЧ-инфекции базируется на трех направлениях:
а) индикация ВИЧ и его компонентов,
б) выявление анти-ВИЧ,
в) определение изменений в иммунной системе.
Среди существующих методов лабораторной диагностики наиболее распространены серологические - выявление антител к антигенам вируса.
В состав ВИЧ входят структурные гены gag (group-specific-antigens), pol (polymerase) и env (envelope), кодирующие трансляцию белков, из которых строится вирус. Группу регуляторных генов ВИЧ составляют tat, трансактиватор всех вирусных белков, rev, регулирующий экспрессию вирусных белков, vif, являющийся вирусным инфекционным фактором, nef - негативный фактор экспрессии и vpx и vpr, функция которых пока не установлена. Ген gag кодирует белки сердцевины вируса и первичным продуктом трансляции его является р53 - белок-предшественник, расщепляющийся на три ( р15, р17 и р 24 ) или с образованием при расщеплении первоначально промежуточного белка р39, который затем расщепляется на белки р17 и р24. У ВИЧ-инфицированных в большинстве случаев образуются антитела именно к этим антигенам, причем антитела к р24 выявляются на ранней стадии инфекции, ибо р24 более иммуногенен, чем р17. Ген роl кодирует белки р51/66 и р31, представляющие собой реверстранскриптазу и эндонуклеазу вируса.
Для выявления антител при ВИЧ-инфекции в основном используют иммуноферментный анализ (ИФА) и иммуноблотинг (ИБ). В первом случае выявляются суммарные антитела к белкам ВИЧ, во втором - к отдельным белкам. В основе ИФА лежит иммобилизация вирусных антигенов на планшетах, на которые сорбируются антитела больного, а комплекс антиген-антитело выявляется с помощью коньюгата антивидового иммуноглобулина с ферментом. Метод довольно специфичен (99%) и достаточно чувствителен (93-99%), позволяет выявлять вирусспецифические антитела у 95% инфицированных. Отрицательные 5% случаев приходится на ранние этапы инфицирования, когда антител еще мало в сыворотке крови или на терминальные фазы болезни, когда организм уже не в состоянии синтезировать антитела в силу резкого истощения иммунной системы. Кроме того в ходе инфекционного процесса наблюдаются периоды исчезновения антител из крови, что также обусловливает отрицательные результаты ИФА. Наоборот, возможны ложноположительные данные ИФА, в основном у больных с аутоиммунными заболеваниями, при инфекции, вызванной вирусом Эпштейна-Барра, когда происходит перекрестная реакция антител к ревматоидному фактору, вирусу Эпштейна-Барра или к молекулам главного комплекса гистосовместимости. Встречаются подобные ложноположительные реакции в 0,02-0,5% случаев.
Сравнительно высокий процент ложно-положительных реакций в ИФА в данном случае объясняется качеством тест-систем, но расхождения даже ниже, чем в экономически развитых странах.
Сейчас внедряется в практику тест-системы 3-4 поколения, в основе которых лежит использование в качестве антигена:
а) лизатов ВИЧ-1,
б) рекомбинантных белков ВИЧ-1,
в) введение антигенов субтипа “О” ВИЧ-1,
г) коньюгаты, позволяющие определять IgM, IgG, IgA.
Все это снижает частоту ложноположительных реакций ИФА при диагностике ВИЧ-инфекции, дает возможность раннего выявления сероконверсии. Улучшение тест-систем, выпускаемых некоторыми фирмами, обусловило более высокую чувствительность, чем иммуноблотинг, используемый для подтверждения специфичности ИФА. Поэтому ИФА с некоторыми тест-системами может использоваться не только как метод для скрининговых исследований, но и подтверждающих.
Антитела к основным внутренним белкам (р17, р24) обнаруживаются у 3/4 инфицированных и примерно у половины больных СПИДом.
Иммуноблотинг используется при диагностике ВИЧ-инфекции в качестве экспертного метода. ИБ сочетает в себе определение антител к отдельным белкам вируса с предварительным электропереносом на нитроцеллюлезную полоску (стрип) антигенов. В ИБ чаще всего выявляются антитела против gp41, обнаружение же в ИБ антител против р24 при профилактических обследованиях не дает оснований для окончательного решения вопроса об инфицировании. Используемый в последнее время рекомбинантный белок для ИБ улучшает оценку результатов.
ВОЗ (1991) предлагает следующий принцип оценки результатов иимунного блота:
а) положительный результат - обнаружение в сыворотке крови антител к двум вирусным белкам из группы env с наличием или отсутствием белков - продуцентов gag и pol,
б) отрицательный результат - отсутствие каких либо антител,
в) неопределенный результат - обнаружение в сыворотке крови антител к белкам из группы gag и pol.
Чаще всего неопределенный результат связан с белками- продуцентами экспрессии гена gag ВИЧ-1 р15/17, р24 и р55, ибо в этих случаях возможны или инфицирование или ложноположительный результат. В подобных случаях, если обследуемый не относится к группе риска, а повторный анализ не дает нарастания титра антител, скорее всего человек не инфицирован. Окончательное же решение вопроса о диагнозе возможно только при проведении более высокочувствительных, экспертных методов исследования: пероксидазной цепной реакции, ДНК-зондов или культивирования вируса. Среди серологических методов в случае неопределенных результатов ИБ используется в качестве экспертной диагностики радиоиммуно-преципитация (РИП).
В основе РИП лежит использование белков вируса, меченых радиоактивным йодом, а преципитаты выявляются с помощью бета-счетчиков. К недостаткам метода относятся дорогостоящая аппаратура, необходимость оборудования для этих целей специальных помещений.
Более доступен метод непрямой иммунофлюоресценции с использованием специальных клеточных линий, инфицированных ВИЧ. Чаще всего используют клеточные линии MOLT, H9, CEM и др. Клетки фиксируют на предметных стеклах с помощью ацетон-метанола, убивающего вирус, но сохраняющего его поверхностные антигены. С последними взаимодействуют антитела сыворотки инфицированного.
Большие трудности интерпретации результатов при перекресных реакциях и в случаях начальных стадий сероконверсии. В первой ситуации при повторном исследовании через определенный промежуток времени антитела не выявляются, а во втором в иммуноблоте появляются новые полосы, свидетельствующие о появлении антител к протеинам или гликопротеидам ВИЧ, характеризуя динамику ответной иммунной реакции на антигены вируса.
Внедрение метода полимеразной цепной реакции существенно обогатили лабораторную диагностику вирусных инфекций, в том числе и ВИЧ-инфекции. Полимеразная цепная реакция (ПЦР) является циклическим процессом увеличения в геометрической прогрессии копии ограниченного синтетическими олигонуклеотидами (праймерами) определенного специфического фрагмента ДНК, протекающей под воздействием термостабильной ДНК-полимеразы при строго заданных температурных и временных характеристиках. Чувствительность ПЦР зависит от специфичности, с которой олигонуклеотиды синтезируют необходимый участок ДНК по отношению к другим неспецифическим участкам нуклеиновой кислоты. Использование различных вариантов ДНК - ДНК-гибридизации с олигонуклеотидными зондами, имеющих ту или иную метку (радиоактивную, флюоресцентную и т.д.) значительно увеличивает чувствительность и специфичность определения продуктов амплификации. Метод гибридизации нуклеиновых кислот весьма высокоспецифичен, однако без проведения амплификации не всегда чувствителен, ибо в крови не велико количество инфицированных клеток. Сочетание двух методов позволило проводить анализ с минимальным количеством материала. В ПЦР может быть использована ДНК, выделенная из свежеполученного материала (кровь, ткани), а также из замороженного, высушенного или фиксированного.
Основным клинико-лабораторным показателем диагностики СПИДа среди ВИЧ-инфицированных в повседневной жизни стало определение содержания CD4+ лимфоцитов: уменьшение уровня ниже 200 клеток/мм является основным критерием постановки диагноза СПИД. Считается, что все ВИЧ-инфицированные лица с количеством CD4+лимфоцитов 200 клеток/ мм и ниже нуждаются как в противовирусной терапии, так и профилактике пневмоцистной пневмонии. И хотя у 1/3 ВИЧ-инфицированных с количеством СD4 + лимфоцитов менее 200 клеток/мм отсутствуют клинические проявления, опыт показал, что у них симптомы развиваются в ближайшие 2 месяца, поэтому они все расцениваются как больные в стадии СПИДа.
В специализированных лечебных учреждениях, в странах с высоким экономическим потенциалом обычно используют комбинацию нескольких лабораторных тестов.
"